Dankzij de vooruitgang in de geneeskunde bereiken steeds meer pediatrische patiënten met een ernstige chronische ziekte tegenwoordig de volwassen leeftijd. Ze moeten dan overschakelen van een pediatrische afdeling naar een ‘volwassen’ afdeling. Hoe organiseren de teams van het Universitair Kinderziekenhuis Koningin Fabiola en het UVC Brugmann zich om de overgang tussen deze twee types behandeling optimaal te laten verlopen? Ontdek het samen met ons …
Om de uitdagingen van deze overgang beter te begrijpen, vertrekken we vanuit een voorbeeld van een kind met een ernstige bloedziekte, sikkelcelziekte. Voor de meeste patiëntjes bestaat er geen behandeling om deze ziekte te genezen. Het is echter wel mogelijk – via een nauwgezette medische opvolging – om de complicaties verbonden aan sikkelcelziekte te voorkomen of behandelen.
“Tegenwoordig bereikt een zeer grote meerderheid van onze sikkelcelziektepatiëntjes de volwassen leeftijd”, aldus prof. Alina Ferster, hoofd van de kliniek voor Hemato-oncologie van het UKZKF. Dat is bijvoorbeeld het geval voor ons patiëntje: hij is ondertussen een adolescent. Zijn lichamelijke problemen, maar ook zijn verwachtingen en bezorgdheden vallen niet langer binnen het domein van de pediatrie en hij zal weldra het UKZKF moeten verlaten. “Om continuïteit in de kwaliteit van de behandeling te garanderen, werken wij vooral samen met de medische teams van het UVC Brugmann”, vervolgt prof. Ferster. “Het UKZKF en het UVC Brugmann vangen al jaren een groot aantal sikkelcelziektepatiënten op. We hebben dus een erkende expertise kunnen opbouwen.”
Van het ene team naar het andere
“ Sikkelcelziekte geeft problemen met het bloed, maar ook de hersenen, het hart, de nieren, de ogen en moeilijkheden op psychologisch en sociaal vlak… Wanneer de patiënt de ene instelling verlaat om naar een andere te gaan, moet heel het multidisciplinaire team rond hem veranderen”, aldus prof. André Efira, honoraris kliniekhoofd in de kliniek voor Hemato-oncologie van het UVC Brugmann. “Wij hebben het geluk op dezelfde campus te beschikken over een groot kinderziekenhuis én een ziekenhuis voor volwassen, die een doorgedreven behandeling voor dit soort bloedziekte aanbieden. We komen vaak samen met onze collega’s van het UKZKF. We praten dan over patiënten die in de nabije toekomst zullen worden behandeld op de dienst ‘volwassenen’ van de afdeling Hemato-oncologie. Wat zijn hun specifieke kenmerken? Welke moeilijkheden ondervinden ze? Hoe zien de pediaters hun verdere behandeling? Ook de liaisonverpleegkundigen van elke instelling hebben voor de transfer van patiënten regelmatig contact. Op die manier wordt de continuïteit van de behandeling gegarandeerd”.
Voorbereiding van de overgang
De overgang wordt altijd voorbereid. Net als onze sikkelcelziektepatiënt zijn adolescenten die naar een volwassen afdeling gaan sinds hun geboorte regelmatig opgevolgd door hetzelfde team. De overschakeling van de ene naar de andere dienst moet dus zo geleidelijk mogelijk verlopen. “We praten erover met de patiënten gedurende ongeveer een jaar, voordat we de fakkel doorgeven aan onze collega’s”, preciseert prof. Ferster. “Bovendien komt een team van het UVC Brugmann minstens eenmaal per jaar naar het UKZKF om de dienst ‘volwassenen’ voor te stellen en de manier waarop de behandeling georganiseerd zal worden, toe te lichten. De pediatrische patiënten worden ook uitgenodigd voor een bezoek aan de afdelingen Hemato-oncologie van het UVC Brugmann.” Vorig jaar zijn overigens voor het eerst ontmoetingen georganiseerd tussen ‘volwassen’ patiënten en pediatrische patiënten die op het punt staan te worden getransfereerd. “Deze praatgroepen gericht op de patiënten waren een onverdeeld succes en leverden vruchtbare uitwisselingen op”, vertelt prof. Efira blij.
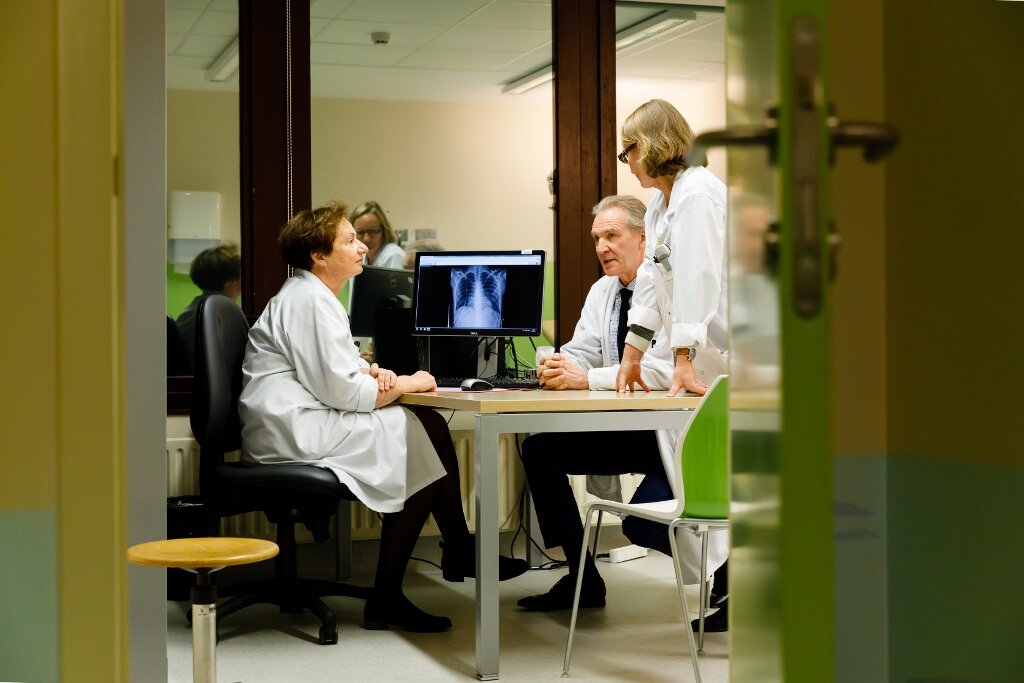
Credits: F. Raevens
5 sleutelfasen: de overgang stap voor stap
Veel afdelingen van de Osiris-campus zijn betrokken bij transfers. Elke afdeling heeft een specifiek traject voor haar patiënten ontwikkeld, maar de grote stappen in het proces zijn gemeenschappelijk voor alle afdelingen. Een voorbeeld.
#1: therapeutische educatie in de pediatrie
Het voorbeeld van sikkelcelziekte
“Op het moment van de diagnose – wanneer het kind nog heel klein is – richten we ons voornamelijk tot de ouders”, aldus Malou Ngalula, referentieverpleegkundige ‘sikkelcelziekte’ in het UKZKF. In een tweede fase richten de teams zich steeds meer tot het kind. “Naarmate de patiënt opgroeit, praat ik direct met hemzelf”, bevestigt Malou Ngalula. “Ik vraag hem hoe hij zich voelt, welke geneesmiddelen hij neemt … Ik baseer mij op zijn dagelijkse leven (school, vrije tijd, excursies …) om samen te zoeken naar oplossingen voor de problemen die hij mogelijk ondervindt. Het doel is het kind opnieuw centraal te stellen in de gesprekken. Dat helpt de overgang die enkele jaren later zal plaatsvinden, voor te bereiden.”
“Op het moment van de overgang naar een dienst voor volwassenen moet de patiënt zijn ziekte kennen, beslissingen in verband met zijn behandeling kunnen begrijpen, weten hoe hij de symptomen onder controle moet houden, in staat zijn alarmsignalen te herkennen en dus weten wanneer hij naar het ziekenhuis moet komen. Kortom, hij moet actor van zijn eigen gezondheid zijn.”
#2: de patiënt als ‘actor’ van zijn gezondheid

Credits : F. Raevens
Het voorbeeld van mucoviscidose
“Al heel vroeg hebben we een georganiseerd en gestructureerd overgangsproces ontwikkeld”, benadrukt dr. Laurence Hanssens, kliniekhoofd van Pneumologie aan het UKZKF. “In de loop der tijd hebben we onze projecten verfijnd. Het proces dat we aan onze patiënten aanbieden, is gespreid over verschillende jaren en heet MOVE UP, als duidelijke verwijzing naar het idee van progressie in de behandeling.”
“Rond de leeftijd van 14 of 15 jaar worden onze patiënten met hun ouders ontvangen door een psychologe van het team. Ze worden uitgenodigd om een vragenlijst in te vullen waarmee een stand van zaken kan worden opgemaakt van hun kennis over de ziekte en de behandeling ervan. De idee is ook de vragen die de patiënt zich mogelijk stelt, de problemen die hem bezighouden, de angsten die hij misschien heeft, enz., te belichten. Deze vragenlijst vormt de basis van de overgang die we later samen met hem realiseren. Gedurende ongeveer een jaar wordt de patiënt in het UKZKF gezien door elk lid van het team (artsen, apotheker, kinesitherapeut, maatschappelijk werker, diëtist, psycholoog …)”, vervolgt dr. Hanssens. “Na afloop van dat jaar wordt hij uitgenodigd om dezelfde vragenlijst nog een keer in te vullen om te evalueren hoe zijn kennis geëvolueerd is. Vervolgens krijgt hij een informatiebrochure die door onze afdeling is opgesteld. In deze brochure wordt het team van het Erasmusziekenhuis voorgesteld, een team waarmee wij nauw samenwerken. We leggen er ook in uit hoe de behandeling zal verlopen gedurende de drie komende jaren, meer specifiek met afwisselend consultaties in elke instelling.”
#3: het doorgeven van de fakkel

Credits : L. Bazzoni
Het voorbeeld van stofwisselingsziekten
“De overgang is een cruciale stap voor de patiënten. Het is een kritieke periode, waarin het risico dat ze aan de behandeling ontsnappen, reëel is. We moeten er dus heel goed op letten dat de overgang van de ene naar de andere dienst optimaal verloopt”, aldus dr. Corinne De Laet, kliniekhoofd op de afdeling Stofwisselingsziekten. “We werken samen met de dienst Interne geneeskunde van het UVC Brugmann”, gaat ze verder.
“We organiseren eenmaal per week gemeenschappelijke consultaties in het UKZKF. De patiënten worden uitgenodigd op twee of drie van dit soort afspraken voordat ze overgaan naar een dienst voor volwassenen. Op die manier leren ze het medisch team kennen dat hen zal opvolgen en krijgen ze informatie over de manier waarop de behandeling zal verlopen en over wat ze zelf zullen moeten doen, enz.”
#4: de patiënt als belangrijkste gesprekspartner
Het voorbeeld van aangeboren hartziekten
De medische behandeling van aangeboren hartziekten is verdeeld over twee verschillende entiteiten. “Een goede samenwerking tussen de teams is essentieel voor een geslaagde overgang”, benadrukt prof. Pierre Wauthy, diensthoofd Hartchirurgie. “Daarom hebben we een pediater (dr. Hugues Dessy) en een cardioloog voor volwassenen (dr. Marielle Morissens), die de verbinding tussen de twee soorten behandeling garanderen.”

Credits : F. Raevens
“In de pediatrie zijn de voorkeursgesprekspartners nog vaak de ouders. Maar tijdens de ‘overgangsconsultatie’ die ik wekelijks in het UKZKF houd, richt ik mij vooral tot de patiënt, zelfs wanneer zijn ouders aanwezig zijn”, aldus dr. Marielle Morissens. “In de praktijk is deze consultatie bestemd voor jongeren van 16 tot 18 jaar met een aangeboren hartaandoening. Maar het gebeurt dat bepaalde patiënten die nog niet klaar zijn om de pediatrische omgeving te verlaten, langer naar deze consultaties blijven komen”, preciseert dr. Morissens. “Deze consultaties zijn voor de patiënten een gelegenheid voor een eerste contact met een cardioloog voor volwassenen in een vertrouwde omgeving, soms in aanwezigheid van een pediater die hen tijdens hun kindertijd heeft opgevolgd. Tijdens deze afspraken stel ik mij voor en leg ik de patiënt uit waarom hij voortaan als ‘volwassen’ patiënt zal worden behandeld. Ik kom ook terug op de hartaandoening waaraan hij lijdt en leg hem de redenen uit waarom hij levenslang moeten blijven worden opgevolgd. Dat is cruciaal om te vermijden dat de patiënt zijn behandeling gaat verwaarlozen.”
#5: de therapeutische educatie gaat door
Het voorbeeld van sikkelcelziekte
Eens volwassen hebben ook sikkelcelziektepatiënten behoefte aan een nauwgezette medische opvolging. “Naarmate de ziekte evolueert, moet de behandeling aangepast worden. Het is cruciaal dat duidelijk uit te leggen aan de patiënt om de therapietrouw te bevorderen”, legt Blanche Dohet, referentieverpleegkundige ‘sikkelcelziekte’ in het UVC Brugmann uit. “De adolescentie is een bijzondere periode voor de patiënt”, voegt ze toe. “Hij zal belangrijke keuzes moeten maken op het vlak van zijn studies, zijn beroepsleven, de plaats waar hij zal wonen … Dat betekent dat hij zal moeten omgaan met veel veranderingen, en tegelijk met de overgang naar een andere afdeling. En dan vergeten we nog dat de adolescentie soms samengaat met een rebelse houding: weigeren zich te identificeren met de ziekte, absoluut willen kunnen leven zoals iedereen … Allemaal parameters waarmee we rekening moeten houden.”
Zich aanpassen aan de patiënt
Het voorbeeld van de diabetologie
De overgang bestaat in de meeste afdelingen van de Osiris-campus al jaren, maar het traject dat wordt aangeboden aan diabetespatiënten is nog maar onlangs ingevoerd. Tot begin juli 2017 had het UKZKF namelijk een dubbele conventie voor diabetologie (voor pediatrische en volwassen patiënten). Een groot aantal volwassen diabetespatiënten werd nog opgevolgd in het kinderziekenhuis. “Het RIZIV heeft echter een einde gemaakt aan deze volwassen conventie in het UKZKF en we werden verplicht op zeer korte tijd een overgangsproces te organiseren”, legt dr. Hakan Bodur, adjunct-kliniekhoofd Endocrinologie in het UVC Brugmann. “Concreet brengt de pediater het onderwerp voorzichtig aan en als de patiënt zich er klaar voor voelt, stellen we hem een eerste gemeenschappelijke consultatie voor. We willen ons echt aanpassen aan zijn ritme!”
“Sommige patiënten zien de overgang als iets positiefs”, stelt dr. Sylvie Tenoutasse, kliniekhoofd diabetologie in het UKZKF, vast. “Deze overgang van de pediatrie naar een ‘volwassen’ behandeling is voor hen synoniem voor autonomie, meer vrijheid. Andere patiënten voelen zich dan weer ‘losgelaten in de natuur’. Daarom is een gepersonaliseerd, aan de patiënt aangepast proces zo belangrijk.”

Credits : F. Raevens
‘Tot ziens’
De relatie die in de loop der jaren is opgebouwd tussen de patiënten en de teams is duurzaam. We leggen hen uit dat onze deur altijd openblijft! Ze weten dat we altijd beschikbaar zijn als ze vragen of zorgen hebben, of als ze ons willen terugzien, dag willen komen zeggen en – wie weet – ons hun partner en kinderen willen voorstellen.
Malou Ngalula
www.huderf.be
www.uvc-brugmann.be
—
Aude Dion
Bron : Osiris News (n° 48, december 2017 – februari 2018)


















